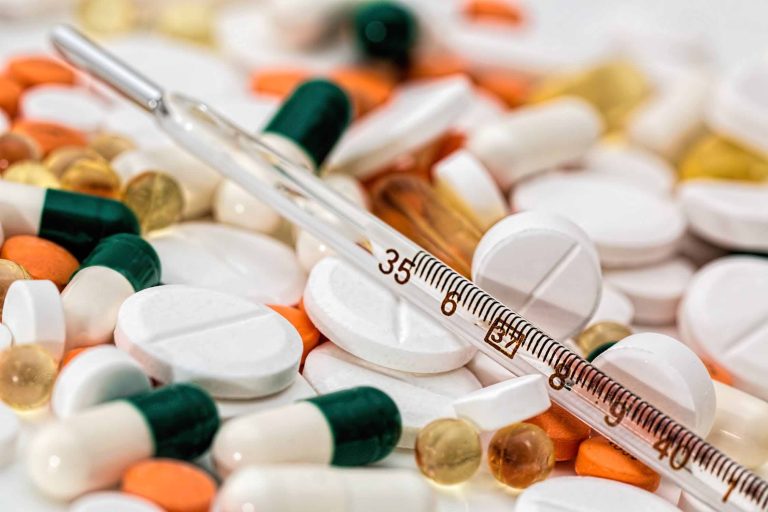
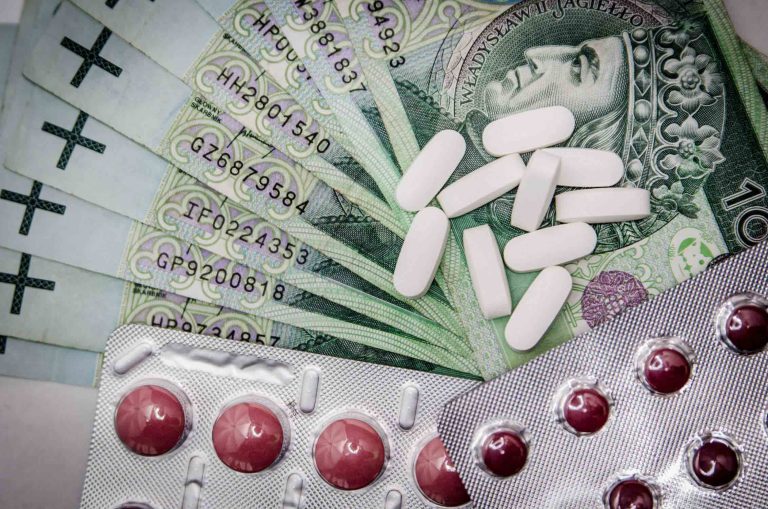
安进帕尼单抗是医保用药吗?据介绍,安进帕尼单抗现在还没有在中国上市,因而也就并不是医保用药。患者假如需要买应用帕尼单抗,现阶段只有选购它在境外上市的版本。现阶段安进帕尼单抗在海外有性价比比较高版本,大家可以联络中国合理合法正规海外医疗服务组织来获得。
帕尼单抗(Panitumumab,英语商品名称:Vectibix)是人源化抗EGFR的IgG2单克隆抗体,能和EGFR的融合阻拦自基因表达和蛋白激酶有关蛋白激酶的活性,能有效缓解直肠癌患者愈后。帕尼单抗帕尼单抗在2006 年9月是由美国FDA审批推出,可以治疗表皮生长因子受体(EGFR)表述呈阳性并且在含氟脲嘧啶、奥沙利铂和伊立替康的化疗方案后病况依然进度或转移直肠癌。帕尼单抗是一种基于人们干细胞疗法的生物制品,现阶段已经在40多个国家被批准。
安进帕尼单抗是医保用药吗?据介绍,安进帕尼单抗现在还没有在中国上市,因而也就并不是医保用药。患者假如需要买应用帕尼单抗,现阶段只有选购它在境外上市的版本。现阶段安进帕尼单抗在海外有性价比比较高版本,大家可以联络中国合理合法正规海外医疗服务组织来获得。
帕尼单抗融合放化疗应用,相比单用放化疗,能够达到一个更好的操纵肿瘤的实际效果,也可延长患者的成活率。帕尼单抗再加上抗化疗的药物也可以加速恶性肿瘤受操纵的时间也。帕尼单抗的适用范围包含:((1)帕尼单抗是一种表皮生长因子受体抗剂可用于单药治疗用或氟嘧啶[fluoropyrimidine],奥沙利铂[oxaliplatin],和伊立替康[irinotecan]化疗方案后肿瘤进展的迁移肠癌。准许是依据无进展生存;并没有材料确认用
帕尼单抗改进病因学病症和增加存活。(2)迁移肠癌实验的回望脾气组剖析对于在密码子12或13里有KRAS基因突变恶性肿瘤患者不曾表明医治经济效益,有这样的基因突变结肠直肠癌的治疗方法不建议用帕尼单抗。