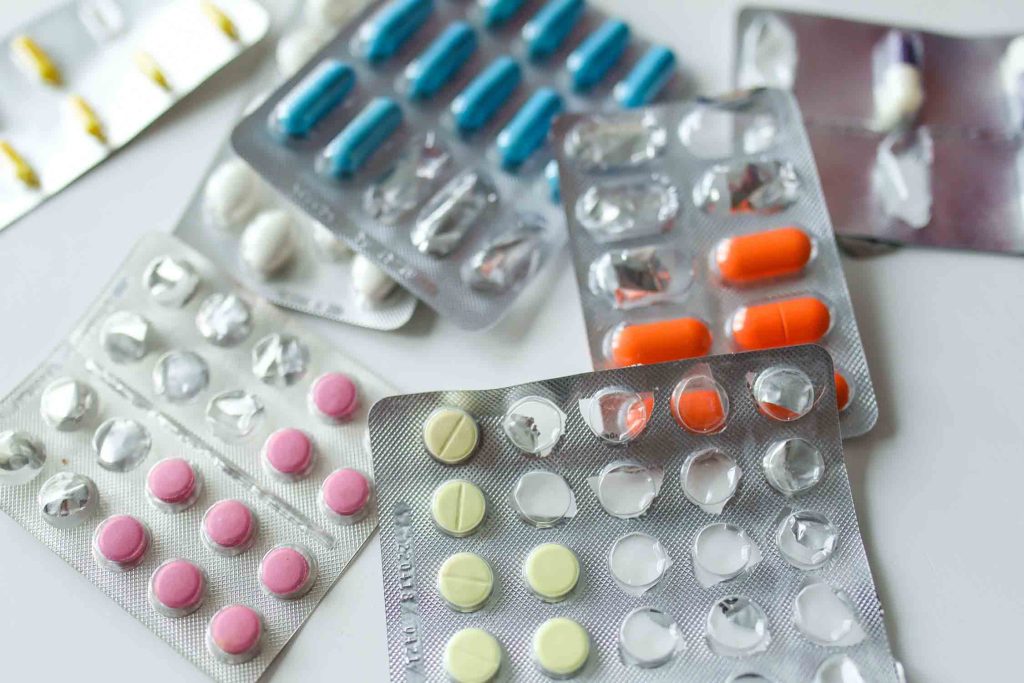
吡咯替尼是由江苏恒瑞医药股份有限责任公司产品研发的新一代靶向治疗HER2蛋白激酶酪氨酸激酶缓聚剂,2018年8月13日,国家食品药品监管质监总局根据其II期临床科学研究結果准许发售,用以HER2阳性肿瘤转移乳腺癌的一线、二线医治。这也是中国第一个根据II期临床科学研究結果获准发售的实体瘤医治药品。吡咯替尼是得到国家科技部“重特大药物研制”重点适用的1.1类创新药,在吡咯替尼的II期科学研究中,对比于对照实验拉帕替尼协同卡培他滨计划方案,吡咯替尼协同卡培他滨将PFS(无病症进度存活期)从7个月显着提高到18.一个月。根据其出色的功效获利,国家药监局有标准准许其发售。
吡咯替尼自面世起就备受关注,2017年,吡咯替尼Ib期科学研究荣获《JCO》(影响因子查询:24.004),它是目前为止唯一一项中国学者在JCO发布的恶性肿瘤药物I期科学研究結果。文章内容一经发刊,便获得国际性著名乳腺癌权威专家的关心,美国加州大学美国旧金山校区研究中心Hope S. Rugo专家教授在《JCO》发帖子觉得吡咯替尼I期科学研究对生物标志物的探寻具体指导着HER2阳性乳腺癌将来精确医治的方位,《柳叶刀・肿瘤学》(Lancet Oncology)杂志期刊也发布了吡咯替尼已在HER2阳性肿瘤转移乳腺癌中展示出优良抗癌活力的社评;同一年12月,吡咯替尼的II期临床科学研究被纳入2017年英国圣安东尼奥交流会(SABCS)本年度大事件回望;2019年6月,吡咯替尼III期PHENIX科学研究登上英国临床恶性肿瘤学好(ASCO)企业年会的口头报告盛典,它是中国自主研发的乳腺癌靶向治疗药物第一次走上ASCO大会;2019年8月,吡咯替尼II期临床科学研究的結果再度被《JCO》杂志期刊特聘全篇发布。
这种成效和认同,高度肯定了吡咯替尼的临床使用价值,也展现了在我国药政改革创新的优秀之处。中国医学科学院附设中医医院马飞专家教授提及:“吡咯替尼是中国自主创新药物研发道上的一个分界点,意味着了中国自主创新药物研发、自主创新药品临床科学研究、精准医学转换科学研究的发展,是十三五期间中国抗癌药物产品研发的意味着”。
吡咯替尼的面世,更改了中国抗HER2医治行业十五年来被海外进口药垄断性的局势,尤其在HER2阳性末期乳腺癌医治行业,曲妥珠单抗经治群体事后治疗方案及功效一直深受权威专家关心,徐兵河专家教授在访谈中提及:“在中国,以往HER2阳性末期乳腺癌的二线靶向治疗服药仅有拉帕替尼,功效不尽如人意,临床上必须 功效更强和安全系数更优质的商品,
吡咯替尼的发生达到了病人急切的临床要求,这也是它能得到国家药监局迅速审核的缘故之一。”
吡咯替尼的II期和III期PHENIX科学研究,均主要表现出了远超目前治疗方案的功效,与此同时具有可承受的安全系数,2019年《中国临床恶性肿瘤学好乳腺癌诊疗指南》以2A类直接证据等级强烈推荐用以末期HER2阳性乳腺癌的二线医治,替代了原来曲妥珠单抗跨线治疗方案,为末期HER2阳性乳腺癌病人给予更优质的医治机遇。这一中国抗HER2行业的提升也将慢慢更改中国临床实践活动。
归功于我国对新药研究关心与帮扶,2015年原我国食品药品安全监管质监总局运行了药物评审审核体制改革,对临床再次的商品给与优先选择评审,大大缩短了药物审核時间。吡咯替尼从2011年4月初次申请办理临床到2018年8月宣布获准,历经仅七年,远短于新药研究动则十多年的均值水平,这毫无疑问是中国药政改革创新的重大进展与成效。